I Migliori Valori De pH e CE

Se conoscere i livelli di pH ed EC vi sembra un passaggio fin troppo complesso per le esigenze di un coltivatore di cannabis hobbistico, vi sbagliate di grosso! Non è necessariamente complicato e può aiutarvi ad ottimizzare le vostre colture domestiche. Abbiamo messo insieme una guida pratica che vi fornirà tutte le informazioni necessarie affinché possiate controllare i livelli di pH ed EC in tutta sicurezza.
COS'È IL pH?
Il "Potentia hydrogenii", o pH, è una scala logaritmica usata per misurare le oscillazioni di acidità e basicità di una soluzione. Il pH assume particolare importanza sia in campo scientifico che colturale. Tuttavia, le differenze emergono al momento di applicare le conoscenze a questa particolare scala di misura.
Nei laboratori di ricerca, il pH viene usato per quantificare il rapporto tra ioni con carica positiva e quelli con carica negativa contenuti in un determinato liquido. In campo colturale, invece, il pH assume importanza al momento di irrigare e concimare le piante. Inoltre, è di fondamentale importanza controllare il pH del substrato colturale, per mantenerlo su valori ottimali.
I valori della scala del pH vanno da 0 a 14, dalla massima acidità alla massima basicità. Il pH 7 è considerato neutro. Al di sotto di questo valore i pH sono acidi, mentre al di sopra alcalini. Esattamente come la scala Richter usata per misurare l'intensità dei terremoti, anche nella scala del pH le oscillazioni di un punto equivalgono ad un fattore 10 volte superiore. Ad esempio, un pH 9.0 è dieci volte più alcalino di un pH 8.0.
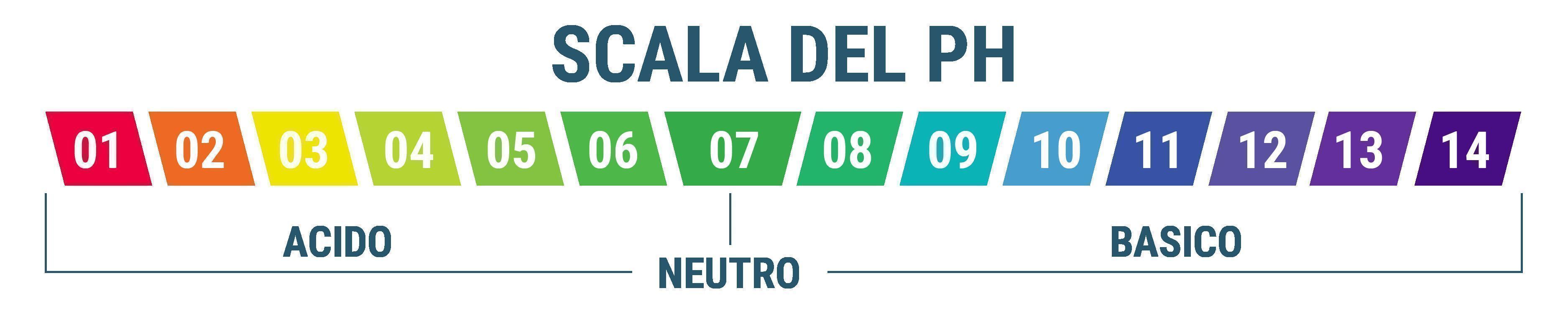
- pH 14: soluzione di soda caustica (1 mol/l)
- pH 13: soluzione di soda caustica (0.1 mol/l)
- pH 11.5: ammoniaca domestica
- pH 10.5: schiuma di sapone
- pH 8.5: acqua di mare, fluidi intestinali
- pH 7.4: sangue umano
- pH 7: acqua pura (neutra)
- pH 6.7: latte
- pH 6: acqua piovana
- pH 5: pioggia leggermente acida
- pH 4.5: pioggia acida, succo di pomodoro
- pH 3: aceto domestico
- pH 2.5: cola
- pH 2: acidi dello stomaco, succo di limone
- pH 1: acido solforoso (acido delle batterie)
- pH 0: acido cloridrico (1 mol/l)
COS'È LA CE?

CE è l'acronimo di conducibilità elettrica. Anche definita con la sigla inglese EC, questo parametro è molto importante per i coltivatori di Cannabis, soprattutto per quelli che usano impianti idroponici, in quanto garantisce il giusto apporto di sostanze nutritive.
In un laboratorio di ricerca, la CE misura la capacità di un materiale di condurre una corrente elettrica. In campo colturale, questo parametro si limita a definire la conducibilità elettrica del substrato e dell'acqua.
Grazie alla lettura della CE, il coltivatore ha la possibilità di definire con maggiore precisione le sostanze nutritive che sta apportando e gli equilibri presenti all'interno del substrato. Riuscire a bilanciare perfettamente tutti i fertilizzanti è essenziale per i coltivatori che vogliono ottenere i migliori risultati, a prescindere dal sistema adottato.
L'unità di misura più usata per definire il contenuto di ioni o sali nell'acqua è il ppm, o parte per milione. Tuttavia, è un'unità usata soprattutto dai coltivatori nordamericani, mentre il resto del mondo preferisce usare le apposite tabelle di conversione da PPM a CE.
Non preoccupatevi se non avete familiarità con le conversioni di conducibilità elettrica. Potete cercarle direttamente su Google e scaricarvele per poterle comodamente consultare in qualsiasi momento. In sostanza, la conversione di un valore PPM a CE serve ad un coltivatore per valutare le giuste proporzioni di sostanze nutritive da aggiungere.
QUALI SONO I MIGLIORI VALORI DI pH E CE?

I valori ottimali di pH e CE per la coltivazione della Cannabis sono condizionati da tre principali fattori: il substrato, le sostanze nutritive e l'acqua. Per i coltivatori che usano terriccio, un pH tra 6.0 e 6.5 è perfetto.
Nelle coltivazioni idroponiche e con cocco, invece, bisogna mantenere valori di pH prossimi a 5.8, o per lo meno non uscire dai margini compresi tra 5.5 e 6.1. I suoli organici o i normali terricci venduti in commercio sono substrati piuttosto tolleranti ed ammortizzano efficacemente le oscillazioni di pH nelle zone radicali delle piante. Al contrario, gli impianti idroponici tendono ad essere molto meno tolleranti ed il pH dev'essere mantenuto sempre su valori ottimali.
I valori della CE sono spesso riportati sull'etichetta dei sacchi di substrato di alta qualità specificamente formulati per la coltivazione della Cannabis. Normalmente, sono riportate anche le proporzioni in % delle varie sostanze nutritive ed una stima delle settimane di concimazione che il terriccio è in grado di offrire alle giovani piante di Cannabis.
I valori di CE possono variare da varietà a varietà di Cannabis. Quelle Indica avide di fertilizzanti, normalmente, prediligono i valori più alti di CE, che possono anche superare 2.5. Le Sativa meno esigenti di concimi, invece, preferiscono una CE più bassa, intorno a 1.0, altrimenti potrebbero rischiare una sovraconcimazione.
L'acqua ha un valore di CE di 0, mentre il pH, normalmente, è neutro, ovvero 7.0. I terricci appositamente formulati per la coltivazione della Cannabis hanno pH 6.0, mentre l'argilla e la perlite usate nelle colture idroponiche sono definite come substrati inerti.
Ovviamente, le coltivazioni idroponiche richiedono molti più accorgimenti e manovre di manutenzione rispetto ad una coltura in terra. I cubetti di lana di roccia devono essere preventivamente immersi in una soluzione al 5.8 di pH prima di essere usati per piantare semi o talee.
I coltivatori di Cannabis più diligenti devono monitorare con estrema attenzione le quantità di sostanze nutritive e i valori di pH e CE, ad ogni concimazione. Bisogna evitare qualsiasi oscillazione di pH e CE.
Il pH dell'acqua dev'essere mantenuto sempre costante, mentre la CE dev'essere aumentata gradualmente man mano che le piante crescono. Ogni settimana sarebbe opportuno un risciacquo del substrato con acqua, per evitare gli accumuli di sali. Questo passaggio è essenziale per i coltivatori idroponici.
La sovraconcimazione è uno dei problemi più comuni nella coltura idroponica, ma ne riparleremo nella sezione sull'idroponia.
Tuttavia, vi anticipiamo che questi problemi derivano da un apporto eccessivo di PPM di sostanze nutritive, il che provoca un aumento di CE.
COME MISURARE pH E CE

In commercio si possono trovare diversi dispositivi per controllare i valori di pH e CE in una coltura di Cannabis. Il nostro consiglio è quello di usare le penne digitali per pH e CE. Con un piccolo investimento, che normalmente non supera i 100€, si può disporre di un dispositivo digitale professionale, con calibrazione e taratura incluse.
Le cartine per misurare il pH da inserire in piccole fiale da scuotere e confrontare con una tabella cromatica possono dare risultati piuttosto precisi, soprattutto quando si coltiva all'aperto e si vogliono usare alternative più economiche. Tuttavia, in un impianto idroponico bisogna essere estremamente precisi e solo i dispositivi più professionali garantiscono una misura perfetta di pH e CE.
COME CONTROLLARE pH E CE
Prima della straordinaria diffusione di Grow Shop e commercio online di prodotti legati al "canna-business", il controllo di pH e CE poteva essere piuttosto impegnativo. Tuttavia, le innovative iniziative del 21° secoli lanciate dagli imprenditori di questo settore hanno messo a punto soluzioni realmente comode ed intelligenti per controllare il pH e la CE.
I più avanzati prodotti concimanti "pH Perfect" della Advanced Nutrients ed alcuni substrati specificamente formulati facilitano il controllo di questi due parametri, ottimizzando l'apporto di sostanze nutritive. I coltivatori che adottano questi fertilizzanti possono anche fare a meno della tecnologia delle penne digitali per pH e CE.
Tuttavia, per coloro che invece desiderano mantenere la massima semplicità nelle loro colture e non possono permettersi fertilizzanti così avanzati e di fascia alta, i dispositivi digitali sono la soluzione migliore e più semplice per controllare questi due parametri.
COME CORREGGERE IL pH E LA CE

La correzione del pH e della CE è estremamente facile e veloce. La maggior parte dei fertilizzanti formulati per la coltivazione Bio della Cannabis, come la linea di prodotti liquidi della BioBizz, tendono ad abbassare il pH neutro dell'acqua, a circa 6.0. Se il pH dovesse scendere sotto questi valori, allora aggiungete 1ml di silicone liquido in 5l d'acqua e dovreste aumentare il pH di 1 o 2 punti.
Tuttavia, se il pH dovesse oscillare verso l'alto, ovvero su valori alcalini di 8.0 o anche superiori, con un paio di ml di aceto di malto diluiti in 5l d'acqua dovreste riuscire a ridurre nuovamente il pH. Ovviamente, in commercio si possono trovare diversi prodotti "pH up" e "pH down". Si tratta di soluzioni specificamente formulate per le fasi di crescita vegetativa e di fioritura e richiedono solo alcune gocce per litro d'acqua per bilanciare il pH.
Anche la CE è piuttosto facile da correggere. Normalmente, il primo passo per risolvere questo problema è aggiungere una buona quantità di acqua per disciogliere gli eventuali accumuli di fertilizzante, il principale responsabile dei valori troppo alti di CE.
Dopo aver realizzato un adeguato lavaggio delle radici, procedete nuovamente a misurare la CE. Se dovesse essere tornata ai livelli ottimali, concimate con un leggero apporto di enzimi e carboidrati, ideali per aiutare le radici a recuperarsi dal lavaggio. In questo modo potrete riprendere a pieno ritmo la vostra coltura.




 Seedshop
Seedshop Headshop
Headshop Vaporshop
Vaporshop Healthshop
Healthshop Smartshop
Smartshop Funghishop
Funghishop Plantshop
Plantshop United States
United States













